- LOGIN
- MemberShip
- 2026-05-07 03:49:06
- Pfizer COVID-19 vaccine for children has been approved
- by Lee, Hye-Kyung | translator Choi HeeYoung | 2022-02-25 05:56:43
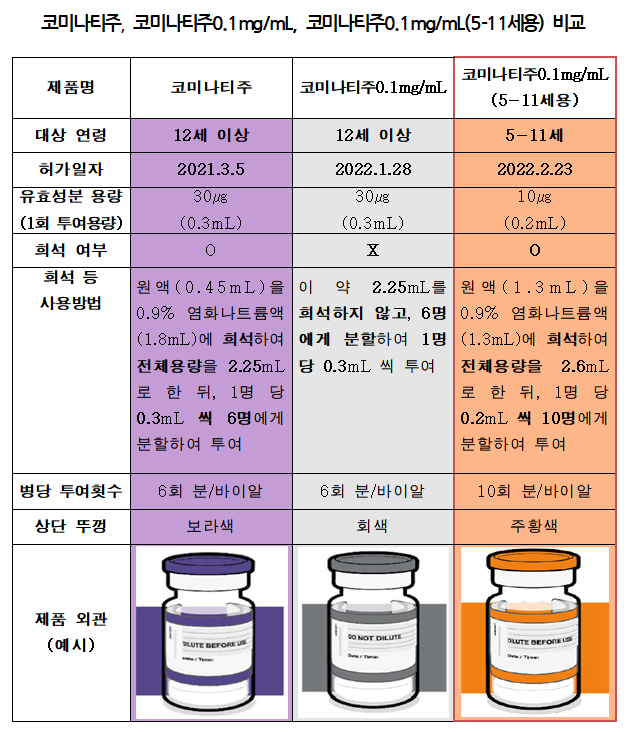
Pfizer's COVID-19 vaccine "Cominatiju 0.1mg/mL," which is subject to vaccination for children and adolescents aged 5 to 11, has obtained an item license.
The MFDS (Minister Kim Kang-rip) announced on the 23rd that Pfizer Pharmaceutical Korea has approved "Comirati 0.1mg/mL" applied for permission as an imported item.
Depending on the design of the clinical trial, different doses were allocated at the age of 11 and 12, and in the case of 5 to 11 years old, the dose was selected in consideration of the results of the immune response obtained from the clinical trial (phase 1).
The vaccine is an mRNA vaccine jointly developed by Pfizera of the U.S.
and Bioentech of Germany and imported by Pfizer Pharmaceutical of Korea, which will be diluted with 0.9% sodium chloride injection.
The most frequent abnormal cases after vaccination were pain at the injection site, fatigue, headache, redness and swelling at the injection site, muscle pain, and chills, and most of the symptoms were mild to moderate.
The probability of redness and swelling at the injection site was 26.4% and 20.%, respectively, higher than 10.3% and 11.4% seen at the age of 16-25 years old.
The abnormal cases appeared more in the second inoculation than in the first inoculation, but were reported to have disappeared within three days of the outbreak.
There were no deaths, myocarditis, pericarditis, or anaphylaxis, and it was confirmed that no serious adverse drug reactions such as drug-related hospitalization or death occurred.
COVID-19 immune responses were compared and evaluated at the ages of 5 to 11 (264) and 16 to 25 (253), and the preventive effect was evaluated as the proportion of patients infected with COVID-19 after administering vaccines (1305 patients) and contrast drugs (663 patients) at the ages of 5 to 11.
As a result of comparing the immune responses of ages 5 to 11 and 16 to 25 at one month after the completion of the second inoculation, it was found that both the ratio of neutralizing antibodies and the serum response rate were proven effective.
As a result of analyzing the preventive effect seven days after the completion of the second inoculation of 1968 people (1305 in the test group and 663 in the control group) who were not infected with COVID-19, the preventive effect of vaccination was 90.7%.
Based on this data, experts agreed that the safety and effectiveness confirmed in clinical trial data can be recognized as a result of consultation by the Central Pharmaceutical Review Committee on the 14th.
However, although it did not occur in clinical trials as a risk management plan after approval, it was decided to observe the safety of myocarditis and pericarditis as a preventive measure, and to collect and evaluate abnormal cases arising from clinical trials and post-authorization use.
Comernaty 0.1mg/mL (for ages 5 to 11) is a vaccine developed and produced separately by Pfizer of the United States for the purpose of preventing COVID-19 aged 5 to 11, and has the same type of additive, usage, and capacity (tojinameran) as previously approved by the Ministry of Food and Drug Safety.
The specific vaccination plan will be announced separately by the Korea Centers for Disease Control and Prevention, taking into account the burden of children's diseases (severe rate, etc.), the epidemic of Omicron mutations, and the schedule of introduction of vaccines for children in Korea.
In the future, the Ministry of Food and Drug Safety plans to analyze the manufacturing and test results of manufacturers for each manufacturing unit of Comirati 0.1 mg/mL (5-11 years old) and check the quality once again with national shipping approval.
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.
- [Reporter's View] Contradiction of "K-passing" and a new drug powerhouse
- Reporter's view | Lee, Jeong-Hwan
- [Reporter’s View] Medical Devices Act binds payment within 6 months
- Reporter's view | Hwang, byoung woo






