- LOGIN
- MemberShip
- 2026-05-07 03:49:18
- Competition in full swing for the ₩100 bil Humira mkt
- by Lee, Tak-Sun | translator Alice Kang | 2022-02-23 05:50:01

On how the market that was once dominated by its only biosimilar option, Samsung Bioepis’ Adalloce, will change with the entry of Celltrion in the market, remains the focus of attention.
Humira, which is mainly used to treat rheumatoid arthritis, has formed a market worth ₩100 billion in Korea.
Celltrion’s Humira (Abbvie, adalimumab) biosimilar ‘Yuflyma pen injection 40mg/0.4mL)’ will be reimbursed from March 1st.
Its insurance price cap was set at ₩244,877, identical to Samsung Bioepis’s ‘Adalloce.’ As the price ceiling for the original drug, Abbvie’s ‘Humira,’ was set at ₩288,091, the price difference between the three products is not large.
Humira recorded $20.69 billion (₩24 .8 trillion) in global sales in 2021 and has maintained the lead in pharmaceutical sales for 10 consecutive years since 2012.
According to IQVIA, the drug also boasted much use in Korea, recording ₩91.2 billion in sales in 2021.
This is a drop from the ₩104 billion sold in 2020, but the decrease was inevitable as Humira’s price cap was reduced by 30% with the approval of Adalloce.
Humira is a monoclonal antibody drug that is used to treat various conditions.
In addition to rheumatoid arthritis, Humira is indicated for the treatment of psoriasis arthritis, axial spondyloarthritis, adult and pediatric Crohn's disease, psoriasis, ulcerative colitis, Behcet’s disease, hidradenitis suppurativa, uveitis, pediatric idiopathic arthritis, and pediatric plaque psoriasis.
With the rapid entry of Humira biosimilars, the industry expects Humira to encounter a crisis within the next two years.
In particular, K-biosimilars are emerging as a vanguard that may break down the stronghold held by Humira.
Samsung Bioepis launched a Humira biosimilar in the European market in 2018 and has been competing for the first and second place in the biosimilar market ever since.
Celltrion is also busy tackling the European market based on the approval it received last year.
In 2023, K-biosimilars’ entry into the Humira market is expected to increase further with Humira’s patent expiry in 2023.
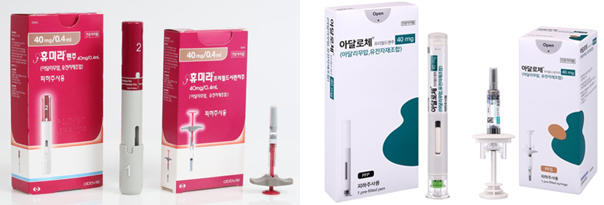
Yuhan Corp, which has a large distribution network, is in charge of its marketing and sales of Adalloce.
With the introduction of Adalloce, Humira’s drug price had also been discounted 30%, and therefore may not be able to guarantee its annual sales of ₩100 billion this year.
In the meantime, competition between AbbVie, which wishes to maintain its market share, and the biosimilar companies Samsung Bioepis and Celltrion is expected to further accelerate with the reimbursement approval granted for Celltrion.
Due to the conservative characteristic of the Korean market, generics or biosimilars generally have difficulty penetrating the Korean market.
In particular, latecomers of injections that are administered in general hospitals like Humira have more difficulty entering the market.
However, as Celltrion’s Remicade biosimilar ‘Remsima’ successfully penetrated the market and earned ₩20 billion in Korea, attention is focused on whether Humira’s biosimilar may also perform this ‘K-magic.’
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.
- [Reporter's View] Contradiction of "K-passing" and a new drug powerhouse
- Reporter's view | Lee, Jeong-Hwan
- [Reporter’s View] Medical Devices Act binds payment within 6 months
- Reporter's view | Hwang, byoung woo






