- LOGIN
- MemberShip
- 2026-05-08 02:17:21
- Did Mooncare truly reinforce coverage for rare diseases?
- by Eo, Yun-Ho | translator Alice Kang | 2021-12-01 05:57:03
The voice requesting expanded coverage for patients with rare diseases had been exceptionally high this year in the 4th year of Mooncare.
Starting with NA discussions held to enhance coverage of innovative new drugs for rare genetic disorders in May by the NA Health and Welfare Committee member Sunwoo Kang, NA members Byungwon Kang, Woni Kim, Young Seok Seo, Hyunyoung Shin held a public hearing to discuss ways to resolve the medically unattended areas, continuing on the effort to foster a policy environment that in which patients with rare diseases are not marginalized.
The main contents that were discussed included the need to apply special exemption of calculation to diseases that are not being covered due to non-designation as a rare disease, and the strong proposal on the need to expand patient access to new rare disease treatments.
The discussion continued to the NA Audit, where the NA Health and Welfare Committee member Sunwoo Kang, and members of the ruling and parties including JaeKeun In and Jongseong Lee all unilaterally urged improvement.
◆100% reimbursement rate for rare disease treatments in 2020? However, the public hearing revealed the different views held by the Health Insurance Review and Assessment Service.
At the public hearing in May, HIRA presented that the reimbursement rate for rare disease treatments was 85.3%(2016~2020) and 100% in 2020.
The numbers indicate that patient access to rare disease treatments is perfect.
But if this is the case, why is the voice to expand reimbursement for rare disease treatments continuing to rise?
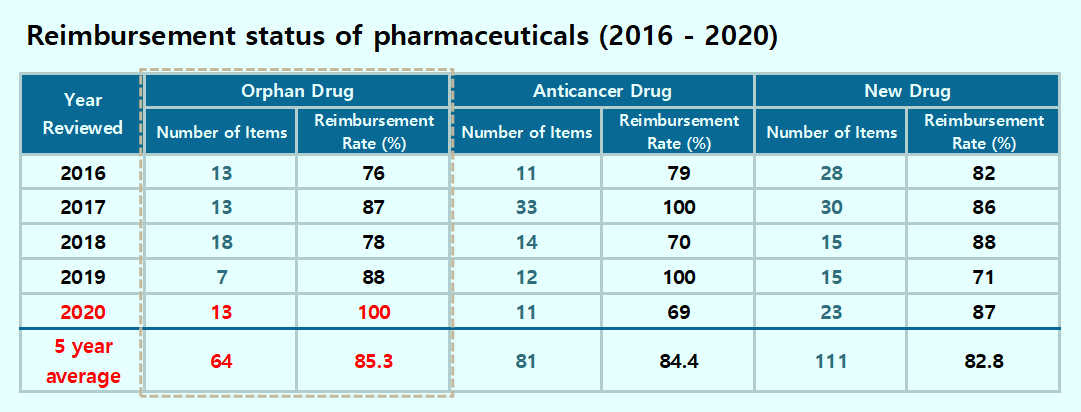
In other words, HIRA’s result excluded various factors including rejected and voluntarily withdrawn items.
Data studied by the Korean Research-based Pharma Industry Association and the Korea Pharmaceutical and Bio-Pharma Manufacturers Association showed that only 50% of the pharmaceuticals that were designated orphan drugs over the past decade were listed on the reimbursement list.
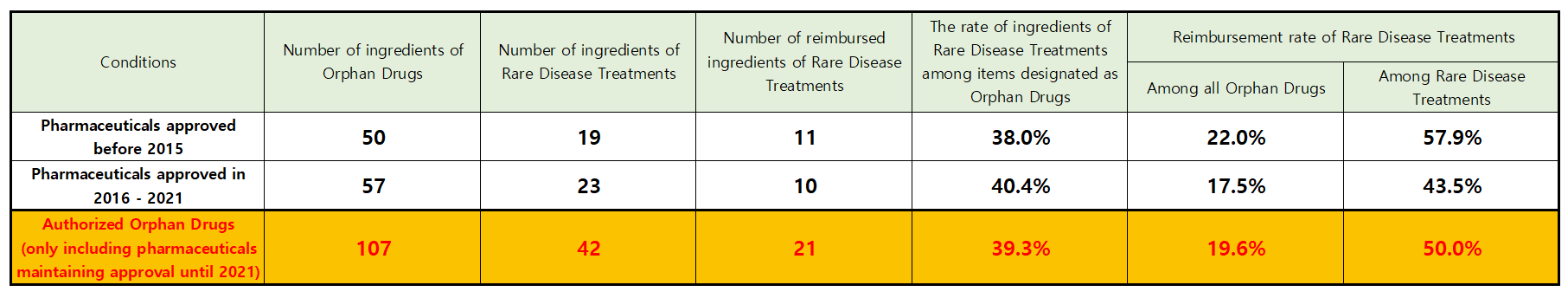
Dailpharm found that KPBMA and KRPIA saw consensus on the need to expand accessibility to rare disease treatments and submitted a statement on the need to expand the pharmacoeconomic evaluation exemption system for rare disease treatments.
In the statement, the two associations pointed out the existence of many rare diseases that greatly affect households with indirect medical costs and deteriorate the quality of life of patients but are not qualified for the ‘life-threatening (less than 2 years of life expectancy)’ condition that needs to be fulfilled to be able to utilize the current special exemption system (RSA and pharmacoeconomic evaluation exemption system) Therefore, the associations insisted that evaluating the ‘clinical need’ only with life expectancy does not take into account the characteristics of rare diseases, and diseases that do not meet the ‘less than 2-year life expectancy’ part of the clinical need requirement should also be allowed PE exemption if it is authorized through expedited approval processes abroad (US BTD, EU PRIME).
The government had said that it would make efforts to improve access to rare disease treatments in the several public hearing and NA audits, but no specific plan or goal seems to be in place.
An industry official said, “The government had recently adjusted the price evaluation criteria of PE exemption drugs by 20% from the lowest A7-adjusted price to improve the price transparency of PE exemption drugs.
If the authorities decided to reduce the risk factors in price as such, they also should increase its scope of benefits.”
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.
- [Reporter's View] Contradiction of "K-passing" and a new drug powerhouse
- Reporter's view | Lee, Jeong-Hwan
- [Reporter’s View] Medical Devices Act binds payment within 6 months
- Reporter's view | Hwang, byoung woo






