- LOGIN
- MemberShip
- 2026-04-13 03:17:18
- Two points to note in Kymriah’s reimbursement process
- by Eo, Yun-Ho | translator Alice Kang | 2022-01-24 05:56:11
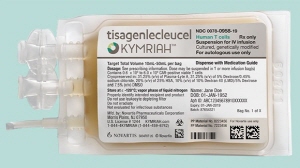
Novartis’s novel CAR-T therapy ‘Kymriah (tisagenlecleucel)’ cleared all the steps necessary for reimbursement under the Health Insurance Review and Assessment Service by receiving approval on its adequacy of reimbursement at the ‘1st Drug Reimbursement Evaluation Committee meeting’ on the 13th this month.
Although another hurdle -the drug price negotiation process with the National Health Insurance Service - still remains, Kymriah’s passing of the DREC review was in itself an encouraging event.
The case is also notable in terms of its speed in review and reimbursement criteria.
◆10 months after MFDS review…Result of ‘longing’ and need Kymirah’s insurance reimbursement listing process was in itself a hot issue.
In its every step from reimbursement application, HIRA’s Cancer Disease Deliberation Committee review, to DREC review, the issue caught the attention of the industry, patients, and the media.
The drug started its reimbursement listing process under the approval-reimbursement evaluation linkage system in March last year after receiving MFDS approval.
6 months later, the agenda was put up for deliberation by the CDDC but deferred.
As soon as the results were released through the media, the Korean Alliance of Patient Organizations among others issued a statement condemning the government and the pharmaceutical company.
The patient association had before criticized the delay in CDDC review of Kymriah’s reimbursement.
Kymriah finally passed the CDDC review in October of the same year.
This was also the first day HIRA disclosed CDDC results.
And then, Kymriah passed review at the first DREC meeting held in 2022.
Statements from KAPO and other associations had poured out at the news of Kymirah’s agenda being deliberated at the DREC meeting.
Another drug that received good news on the same day with Kymriah was MSD’s immunotherapy drug ‘Keytruda (pembrolizumab),’ which awaited 5 years (to extend its reimbursement to first-line in non-small-cell lung cancer).
For patients in dire need, even the 10 months spent waiting for Kymirah would have been too long.
However, considering the average time spent on listing innovative new drugs in Korea and even taking into account the disease and number of patients that benefit from the two drugs, Kymriah’s reimbursement progressed quickly.
This progress is highly likely due to a combination of the patients’ ‘desperate longing’ and execution ability.
The government would have felt some burden.
In addition, Novartis Korea’s efforts in presenting a fiscal-sharing plan through the persuasion of its headquarters are also expected to have played a part.

Kymriah’s indication is for the treatment of ▲ adult patients with relapsed or refractory diffuse large B cell lymphoma (DLBCL) after two or more lines of systemic therapy, and ▲ patients up to 25 years of age with B-cell precursor acute lymphoblastic leukemia (B-ALL) that is refractory or in second or later relapse.
Kymriah, which is going through the reimbursement listing process through the pharmacoeconomic evaluation exemption system, is applied the expenditure cap type of Risk Sharing Agreement (RSA) scheme.
As it is an ultra-high-priced new drug, the prevailing industry assumption was that additional restrictions would be set for its reimbursement in addition to the expenditure cap.
This is in line with the government’s plan to converge performance-based type and the expenditure cap type of RSA as an alternative necessary for expanding coverage of high-priced new drugs.
As expected, the performance-based type was additionally applied to the DLBLC.
indication.
The performance-based type limits reimbursement of drug expenditures according to treatment effectiveness after administration.
However, no other options were set to restrict reimbursement of Kymriah other than the expenditure cap for the B-ALL indication.
Although limited to B-ALL, this could be seen as the government’s allowance of a freer administration of Kymriah in the disease.
In such various aspects, Kymriah’s every step of the reimbursement progress is receiving attention Whether the effective but expensive Kymriah can push through the remaining processes and get its name on the reimbursement list remains to be seen.
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.





