- LOGIN
- MemberShip
- 2026-05-11 13:21:11
- About 70% of new anticancer drugs are listed
- by Lee, Hye-Kyung | translator Choi HeeYoung | 2020-06-11 06:22:35
The average listed rate for new drugs approved in Korea was 67.2%.
Looking at the rate of chemotherapy drug listed alone, it was 70.2%, which is higher than all new drugs.

As a result of analyzing 570 new drugs approved in Korea from 2007 to 2018 by the Korea Institute for Health and Social Affairs, Trends in new drug properties seen in the global market have recently been observed, such as increased treatment for severe diseases, higher costs, and uncertainty in the basis for decision making.
As a result of analyzing the database of the MFDS, the annual average of 47.5 new drugs has been approved over the past 12 years.
Of these, 141 new anticancer drugs accounted for 24.7% of all new drugs, and since 2007, the proportion has increased gradually, accounting for about 39% in 2016 and 2017.
As a result of comparing the health insurance drug price file and claim data based on the MFDS, as of May 2019, 383 items, 67.2% of the 570 new drugs approved, were listed on the reimbursement list.
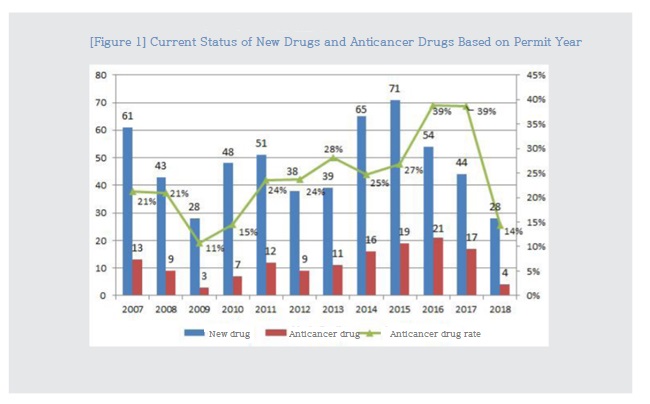
Anticancer drugs that were approved in 2013~2015 have a very high guarantee rate of about 90%, and the incidence rate of approved anticancer drugs after 2016 is likely to increase further.
Among the new drugs for anticancer drugs, 45.5% of them were listed as risk-sharing agents (RSA).
In particular, the ratio of RSA to reimbursement was more than 90% in the case of licensed anticancer drugs from 2016 to 2017, after the policy to strengthen the guarantee in 2014.
In the United States or the European Union, the percentage of drugs approved for sale under conditional approval was the highest in RSA-listed new drugs at 66.7%, with 46.8% for anticancer drugs and 15.4% for all new drugs.
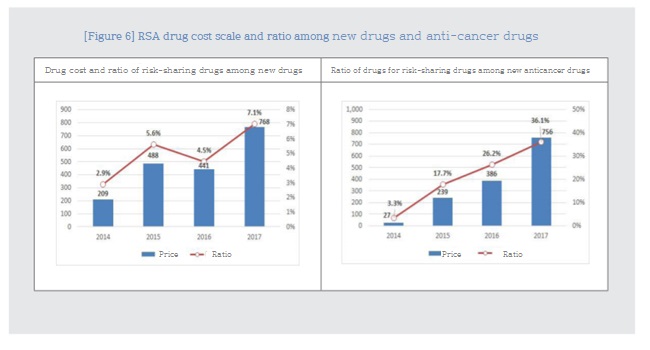
Among the new drugs in 2014, the RSA drug cost was ₩20.9 billion, accounting for 2.9% of the total new drug cost, while in 2017, the value rose to ₩76.8 billion and 7.1%, respectively.
The cost of RSA in anti-cancer drugs increased rapidly from 3.3% of total anti-cancer drug drugs to ₩2.7 billion in 2014, to ₩75.6 billion in 2017 and 36.1%, respectively.
If the new drug listed in 2012 took 97 days to be used for the first time in advanced general hospitals, it was shortened to 28 days in 2017.
%.
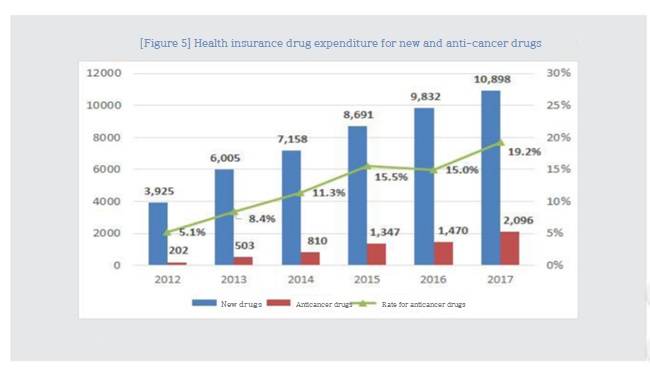
As a new drug for anticancer drugs, the proportion of total drug expenditures for products with less than 6 years of entry into the drug increased from 0.35% in 2013 to 0.91% in 2017, and also increased annually.
"The proportion of anticancer drugs in the number of new drugs and the expenditure of new drugs is increasing, and new drugs registered as RSA are increasing," said the Korea Institute for Health and Social Affairs.
The institute said, "We need a policy to secure financial continuity by strengthening the clinical efficacy evaluation structure of new drugs in our decision to manage uncertainty in new drugs and secure access to innovative new drugs."
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.
- [Reporter's View] Contradiction of "K-passing" and a new drug powerhouse
- Reporter's view | Lee, Jeong-Hwan





