- LOGIN
- MemberShip
- 2026-05-10 13:29:09
- Cyramza OS Clinical 9.6 months vs. RWE 7.9 months
- by Lee, Hye-Kyung | translator Byun Kyung A | 2020-11-17 06:26:30
Apparently a study in South Korea comparing the clinical trial result and real world data has found a targeted therapy for stomach cancer Cyramza (ramucirumab) and a targeted therapy for breast cancer Kadcyla (trastuzumab) have shorter overall survival in the real world.
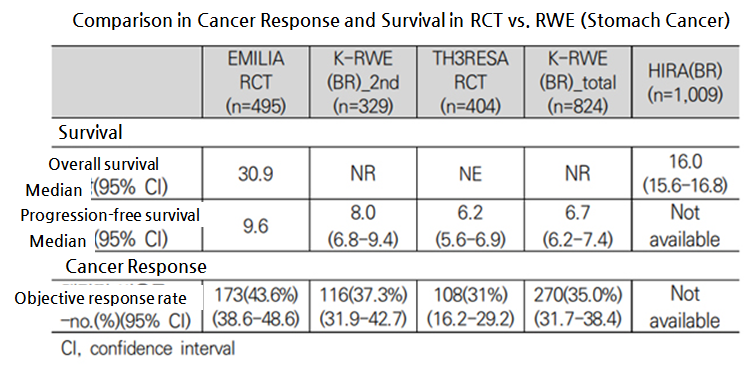
The clinical trial report on Cyramza stated its overall survival (OS) reached 9.6 months (8.5-10.8), but a statistic claim billing analysis by the Health Insurance Review and Assessment Service (HIRA) found the figure to be at 7.9 months (6.3-8.4), and it marked 10.0 months (9.3-10.7) in an analysis on medical record archived by research participating hospitals.
As for Kadcyla with insufficient period of monitoring, patients’ progression-free survival (PFS) was compared and found the initial clinical trial result was at 9.6 months, which was 1.6 months longer than the actual medical record analysis at 8.0 months (6.8-9.4).
The said gaps between clinical trial result and real-world data (RWD) was verified in the Retrospective Study on Designing the Real-world Evidence (RWE) Platform for Improved Pharmaceutical Reimbursement Management (Principle investigator: Dr.
Kim Dong-suk and Dr.
Byun Ji-hye) published by HIRA on Nov.
12.
HIRA selected Lilly’s Cyramza (ramucirumab) and Roche’s Kadcyla (trastuzumab) as subjects for RWD-basis outcome study to generate RWE.
The research was conducted as randomized controlled trial (RCT), the same method the pharmaceutical companies have used, when listed the drugs, by collecting and analyzing medical records from 242 healthcare providers (68 hospitals) associated with Korean Cancer Study Group.
◆Cyramza: The RCT evidence used when listing for the healthcare reimbursement compared the paclitaxel single therapy against Cyramza in combination with paclitaxel, which confirmed the combination therapy’s efficacy, statistically.
Based on the billing data collected from May 2018—the point of Cyramza listing—through December 2018, the fatality rate in patients with a record of Cyramza prescription, from the point of first stomach cancer diagnosis to death, was reviewed.

The median OS was approximately 240 days (7.9 months), which was shorter than 9.6 months from the original RCT.
The majority of the patients, or around 55% of them, were administered with the drug four times or less, followed by the number of patients who used the drug five to six times and over 10 times.
The average number of administration marked 5.3 times among all patients.
Analyzing the impact of variables affecting the OS with Cox proportional hazards model, the OS was statistically better when the diagnosis was given over a year ago, administration period was over 12 weeks, the number of administration was over seven times, and when it was at tertiary hospitals.
The outcome study on electronic medical record (EMR) analyzed patient survival after using Cyramza with Kaplan-Meier estimator.
The study concluded the time to progression (TTP) to be at 4.2 months, PFS at 4.03 months and OS at 10.03 months.
The RWE based on these RWD confirms Cyramza in combination with paclitaxel showed shorter OS, compared to the original RCT.
◆ Kadcyla: Apparently, 331 out of 1,009 patients have died among the patients who were administered with Kadcyla at least once for year since the point of listing in August 2017 through July 2018.
The median OS was approximately 449 days (15 months), which was shorter than both 29.9 months (Dieras et al, 2017) and 22.7 months (Krop et al, 2017) demonstrated in the company’s RCTs.
But HIRA said there is a limitation with the insufficient time of monitoring as the drug received the reimbursement only from August 2017.
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.
- [Reporter's View] Contradiction of "K-passing" and a new drug powerhouse
- Reporter's view | Lee, Jeong-Hwan
- [Reporter’s View] Medical Devices Act binds payment within 6 months
- Reporter's view | Hwang, byoung woo






